Quand rechercher un déficit immunitaire en cas d’eczéma ?
Les déficits immunitaires peuvent être classés en primitifs et secondaires. Les déficits immunitaires secondaires sont dus à des maladies, des traitements ou encore des infections. Ils concernent essentiellement les adultes. Les déficits immunitaires primitifs sont des maladies héréditaires dont plus de 200 différentes ont été décrites ; près de 180 anomalies génétiques sont connues. Ils concernent 1 naissance sur 5 000 et le diagnostic est fait principalement chez les enfants.
Le déficit peut toucher la réponse immunitaire non spécifique ou innée (cellules du système monocyte-macrophage, protéines du complément) ou la réponse immunitaire spécifique ou encore adaptative (lymphocytes T, lymphocytes B). Une classification est présentée dans le tableau I [1]. La plupart de ces déficits immunitaires sont symptomatiques dès les premières années de vie.
Syndrome hyper-IgE dominant ou syndrome de Job-Buckley
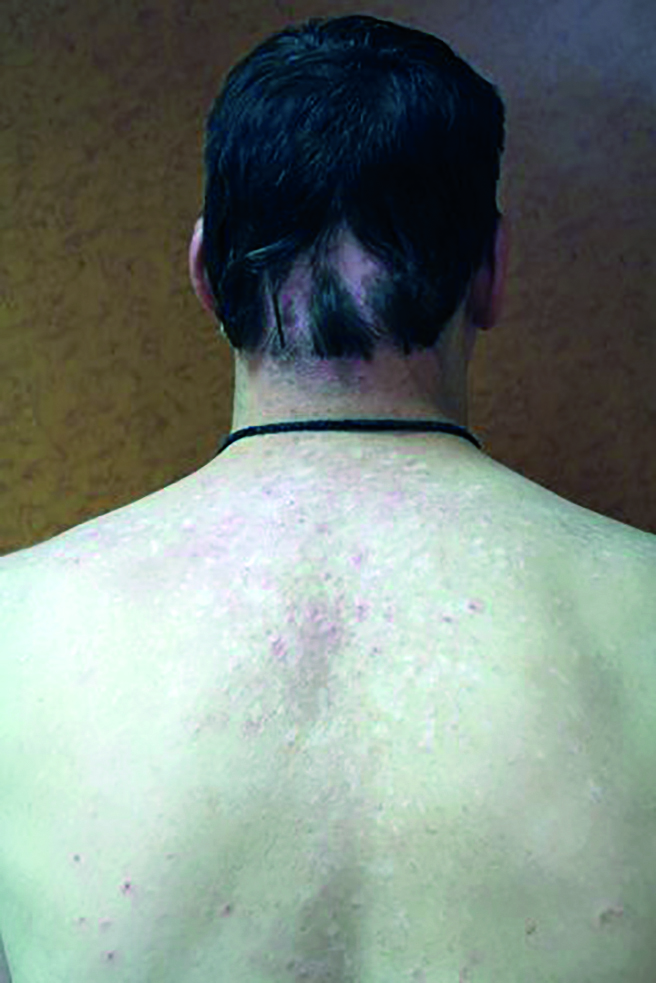
Le syndrome hyper-IgE dominant, ou syndrome de Job-Buckley, se manifeste par un eczéma précoce (dès le premier mois de vie) habituellement résistant aux dermocorticoïdes, puis par des papulo-pustules du visage et du cuir chevelu et un aspect de prurigo du tronc et du cuir chevelu (fig. 1). Les patients atteints présentent également des infections récidivantes à tropisme cutané et pulmonaire avec des abcès froids, des séquelles pulmonaires fréquentes et une atteinte candidosique (plus tardive) généralement résistante et étendue. Les autres signes comportent une dysmorphie faciale avec un nez épaté et un front proéminent, des anomalies dentaires et un retard mental inconstant. La transmission est autosomique dominante (1 à 9/100 000) et la mutation identifiée est STAT3p. K558E [2].
Fig. 1 : Patient présentant un eczéma avec aspect de prurigo du tronc dans le cadre d’un syndrome hyper-IgE dominant ou syndrome de Job-Buckley.
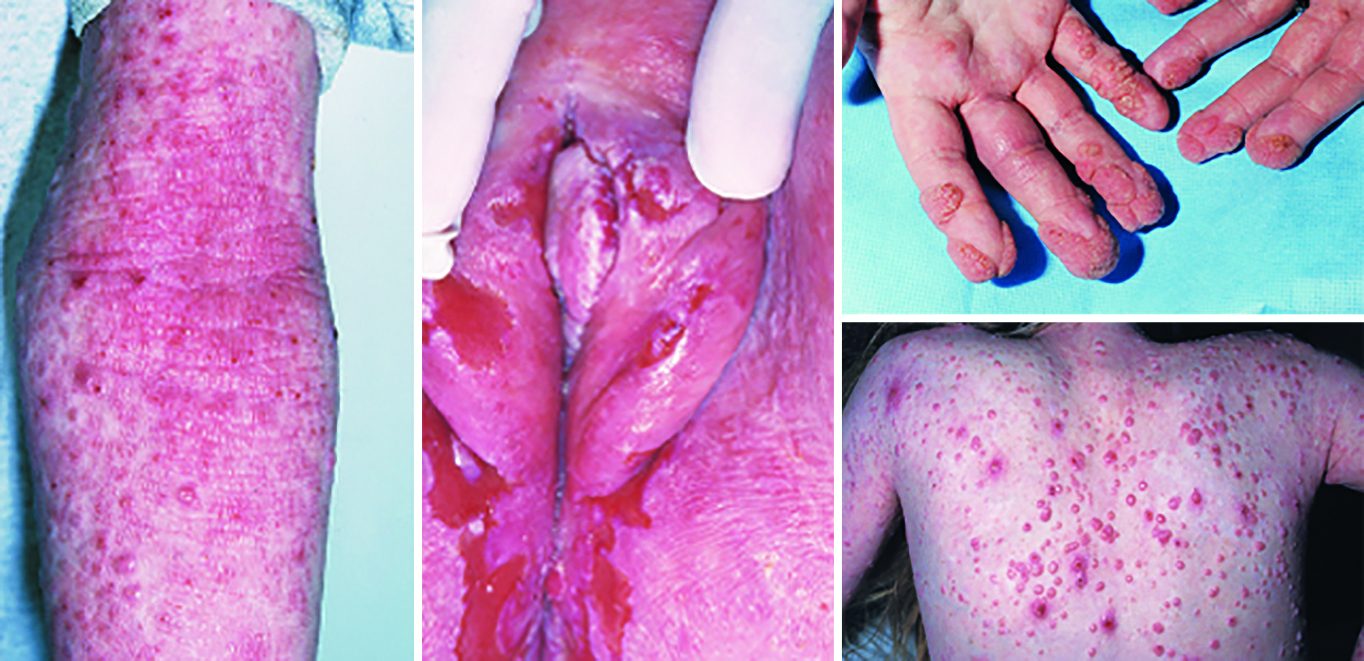
Fig. 2 : Patients avec un syndrome hyper-IgE récessif (mutation DOCK8) [d’après 2].
Syndrome hyper-IgE récessif
Le syndrome hyper-IgE récessif se manifeste par une atopie sévère souvent localisée au siège, des infections à herpèsvirus et papillomavirus chroniques et des Molluscums contagiosum multiples. Les infections sont également fréquentes : infections bactériennes cutanées à staphylocoque doré, pneumopathies, otites et sinusites (fig. 2) [3]. La mutation identifiée est DOCK8, protéine qui a un rôle dans le cytosquelette des lymphocytes.
Déficit immunitaire combiné
Le déficit immunitaire combiné est caractérisé par des lésions eczématiformes, sur le mode érythrodermique en période néonatale, des infections sévères, une diarrhée et une cassure de la courbe staturo-pondérale. La forme sévère est une urgence diagnostique compte tenu de l’absence totale de lymphocytes. Dans la forme non sévère, le nombre de lymphocytes T est normal ou diminué mais avec une fonction anormale et le nombre de lymphocytes B est diminué ou pas. La transmission est liée à l’X ou autosomique récessive.
Syndrome de Wiskott-Aldrich
Le syndrome de Wiskott-Aldrich se manifeste par un eczéma précoce, étendu, résistant aux dermocorticoïdes, des infections bactériennes, virales et candidosiques récidivantes et sévères (Molluscums contagiosum très étendus) ainsi qu’un purpura, des affections auto-immunes (anémie, neutropénie) et une diarrhée sanglante. La transmission est liée à l’X, avec une mutation du gène WASP. Elle concerne 1 cas pour 4 millions de naissances de garçons.
Quand évoquer un déficit immunitaire ?
On évoquera un déficit immunitaire devant :
-
- une dermatose inflammatoire chronique particulière : sévère, résistante aux traitements classiques, renforcement tête et cou, plis ;
-
- des infections (bactériennes, virales, candidosiques) particulières : précoces, sévères, récidivantes ;
-
- des manifestations associées ;
-
- un caractère familial.
En cas de suspicion de déficit immunitaire, on demandera un hémogramme, un dosage pondéral des IgG, IgA, IgM et IgE et une électrophorèse des protéines plasmatiques. Les examens plus approfondis (immunophénotypage lymphocytaire, tests fonctionnels lymphocytaires spécifiques et non spécifiques, etc.) seront à discuter avec le collègue hémato-pédiatre ou immunologiste.
Bibliographie
- Picard C, Al-Herz W, Bousfiha A et al. Primary Immunodeficiency Diseases: an Update on the Classification from the International Union of Immunological Societies Expert Committee for Primary Immunodeficiency 2015. J Clin Immunol, 2015;35:696-726.
- Minegishi Y, Saito M, Tsuchiya S. Dominant-negative mutations in the DNA-binding domain of STAT3 cause hyper-IgE syndrome. Nature, 2007; 448:1058-1062.
- Zhang Q, Davis JC, Lamborn IT et al. Combined immunodeficiency associated with DOCK8 mutations. N Engl J Med, 2009,19;361:2046-2055.
Rédigé par les Drs Emilie Brénaut et Justine Daguzé, d’après la communication du Dr Catherine Droitcourt (CHU Pontchaillou, RENNES).
MAJ : 26 octobre 2018